究竟是什么限制了电池容量?

自上世纪 60 年代以来,集成电路上可容纳的晶体管数目,约每隔两年便会增加一倍。换个说法是18个月便会将芯片的性能提高一倍,这就是我们所熟知的摩尔定律。得益于此,消费电子产品在过去 60 年里快速小型化并普及开来。然而,与半导体和电子领域的指数级进展形成鲜明对比的是电池化学/材料领域的缓慢进步。
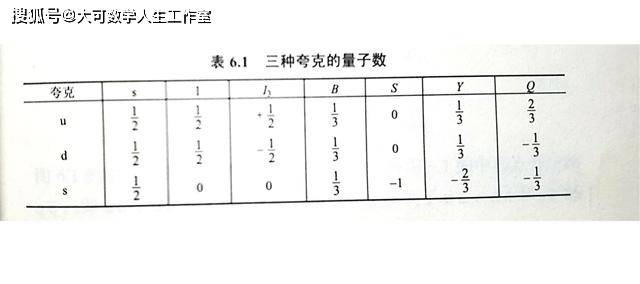
如果我们以 1859 年普朗特发明首个实用型可充电电池铅酸蓄电池为起点,假设其能量密度的演化(~1 Wh/kg 或 3600 J/kg)受摩尔定律的控制,那么到 1928 年,储存在 1 公斤电池中的能量将等于第一颗原子弹的爆炸能量(~10^11 Wh 或 ~10^14 J );到 1950 年,可以从电池质量转换的能量将等于根据爱因斯坦的质量能量方程 E=mc^2 计算得出的能量(~ 10^13 Wh 或 ~ 10^16 J)。并且照这个趋势继续下去,那么在一个世纪内,这一数字将变成真正的天文数字。但是现实是,电池的能量密度相较其最早发明时并没有指数级的跃升,自1970年以来,平均增长率仅约 5%。
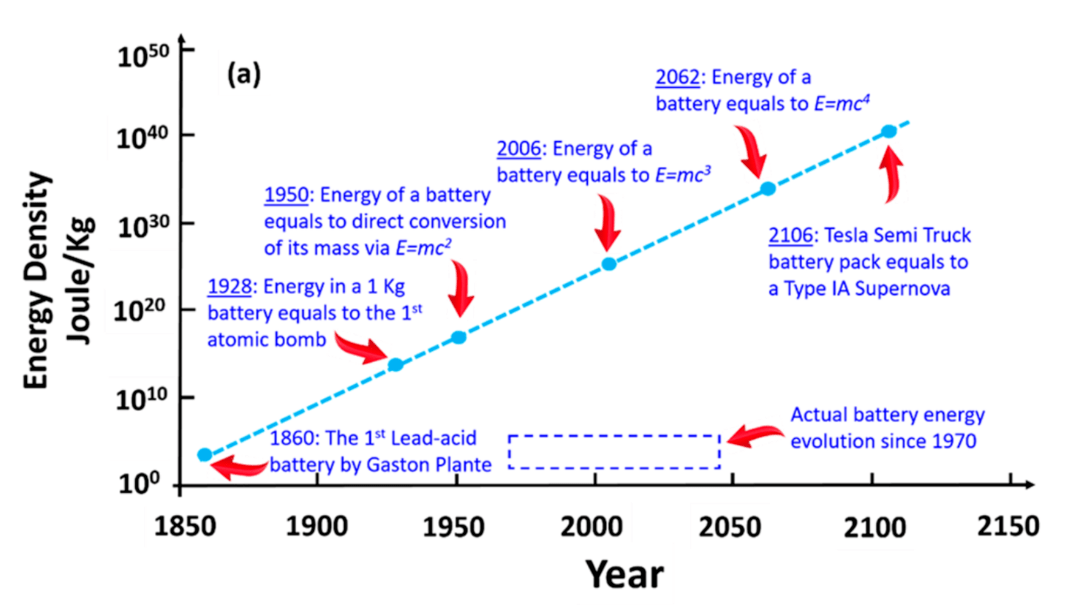
以 1970 年以来的实际电池能量密度增长为例,早期发明的镍镉、镍氢电池变化不大,90 年代后量产的锂离子电池虽然拥有比前代的镍镉、镍氢电池更大的能量密度,但在之后 30 年的发展中,也难以突破 400 Wh/kg 的上限。即使是能量密度更高的锂金属电池,也只是达到 500 Wh/kg 的级别。
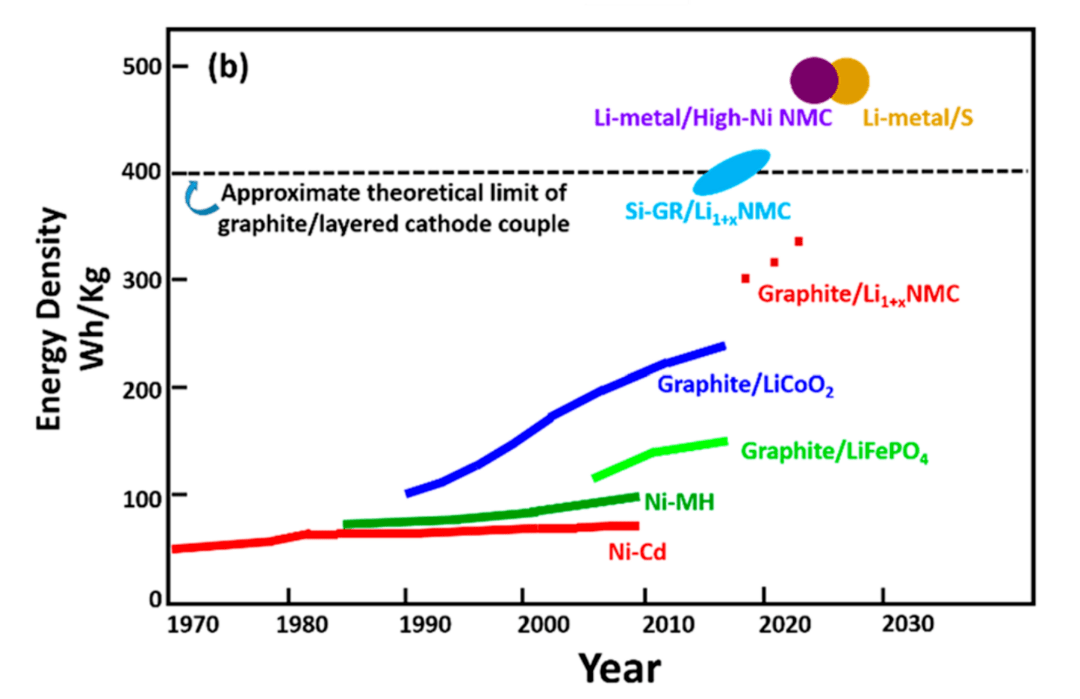
如果我们将锂离子电池的能量密度与其他物质相比较,可以看到,在下面的坐标系中,锂离子电池位于最左下角。而汽油、柴油、煤油、天然气等燃料所使用的碳氢化合物显然具备更高的能量密度。这意味着,我们目前所依赖的电池在化学物质本身的能量密度上就具有天然的劣势。

那么能不能换一种能量密度更高的新类型的电池呢?很遗憾,以锂元素为代表的电池,已经是伏打发明第一个电池以来,我们目前所能量产的最具潜力的电池。在所有金属中,锂的原子序数最低,因此原子量最小,密度最低。同时锂属于碱金属,也是最活泼的金属之一。1913 年,吉尔伯特·路易斯和弗雷德里克·凯斯经过实验得到了锂的精确电位,并宣称锂是具有最高电极电位的电极材料。小原子量、极低的还原电位和单价电荷的偶然组合,使得锂具有其他元素或化合物几乎不可能匹敌的独特性质。凭借这种优势,锂在过去五十年中基本上主导了寻求更高能量密度电池的努力。
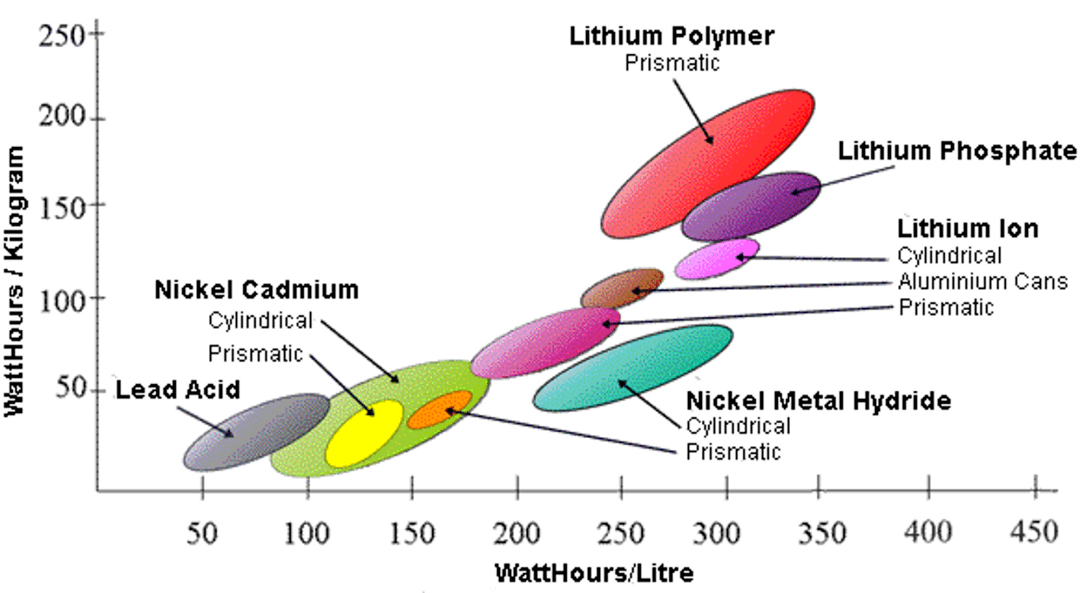
而在实际应用中,锂离子电池以及类似的化学储能型电池背后的基本化学原理,又进一步限制了电池的能量密度。可以看到以锂与氧气反应和实验中的锂空气电池为例,其质量能量密度为 43 MJ/kg,但在实际量产中的锂电池和锂离子电池的质量能量密度便极速下降。
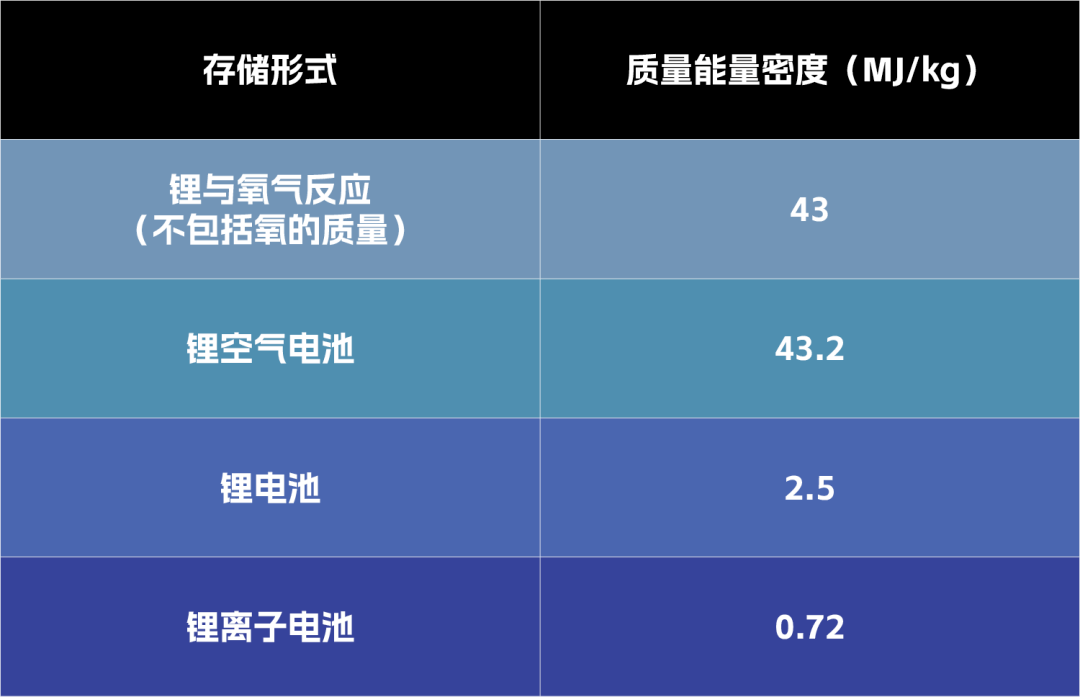
这是为什么呢?我们都知道电池的本质是其背后的氧化还原反应,在此期间电子会在外部电路定向移动形成电流。而我们对于电池的需求,除了能够提供电能以外,还需要它能够重复充放电,并且足够安全。而要做到这一点,就要求电池内部的氧化还原反应是可控有序的,这一点就将电池与燃料物质的化学反应区分开来。燃料燃烧时也会发生氧化还原反应产生能量,但其中的电子转移是无序不可控的。为了有序的电子转移,电池不得不携带没有能量但是必不可少的电解质以及各种辅助材料,于是进一步降低了自身的能量密度。

在锂离子电池之前,1980 年代首先量产的其实是锂金属电池。典型代表是 Moli Energy 公司销售的 AA 电池。但是由于锂过于活泼,极易发生我们所不希望的副反应,形成锂枝晶,造成锂金属电池短路自燃。这使得使用锂金属电池的手机发生多起起火事件,Moli Energy 也因此破产,标志着研发锂金属电池的主流努力的结束。

退而求其次的便是我们今天广泛使用的锂离子电池。不再使用锂金属作为电极,而是使用石墨负极和各种锂化合物作为正极,放电时锂离子从石墨负极脱出嵌入正极材料中,充电时锂离子再由正极脱出嵌入石墨负极。相比锂金属电池,锂离子电池本身真正能够提供能量的含锂量又进一步下降。
同时,为了保证反应的正常进行,锂离子电池内部有大量并不贡献容量却必不可少的材料,例如电解液、隔膜、集流体等;并且,如果正极材料上的锂离子全部参与反应,正极材料的晶体结构将会被破坏,导致电池容量发生不可逆下降,因此,锂离子不能从电池正极材料中完全脱出,也就是说有相当一部分锂离子本身也不能贡献能量;另外,锂离子脱出过多的正极材料稳定性较差,易发生热失控导致电池燃烧,因此锂离子电池内部还需要额外的不贡献容量的零部件结构以保证电池的安全性。
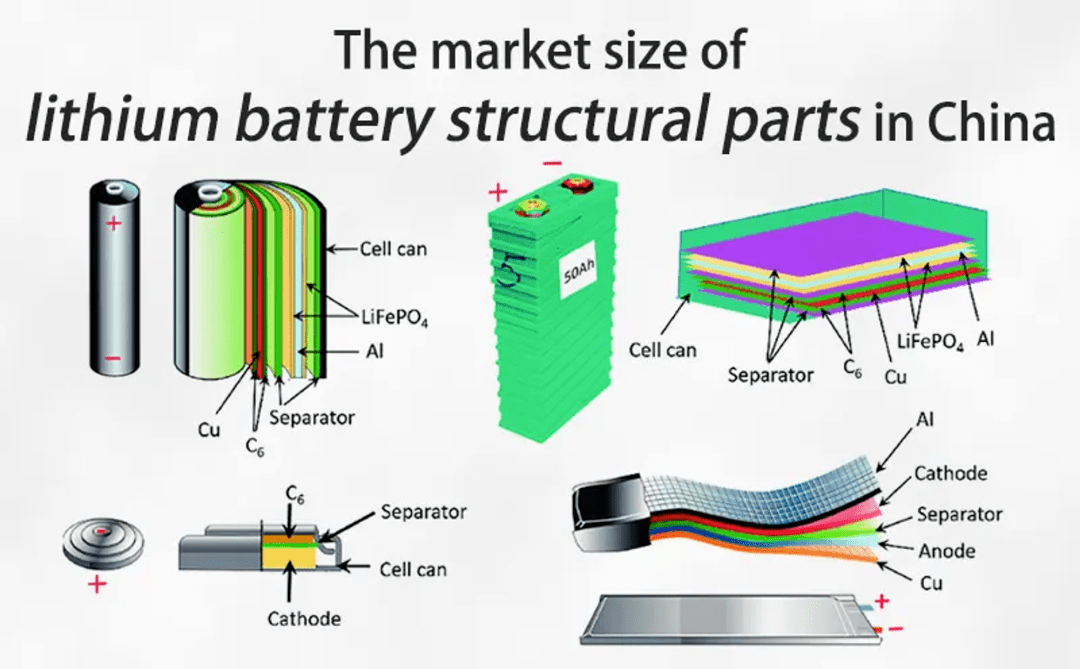
电池界流传的有一句格言,“给定最好的正极、负极、隔膜和电解质,只需将它们组合在一起,就可以生产出最差的电池”。我们所能安全掌控的用来制造电池的化学物质本身的特性,注定了电池材料的开发是一项极具挑战的工程。自从两个多世纪前伏打组装出第一块电池伏打电堆以来,只有不到 20 多个电池系统(一次电池和可充电电池)成功商业化。虽然电池只由三个主要活性成分组成:正极(阴极)、负极(阳极)以及以离子方式连接电极的电解质。这样的配置看似简单,但事实上,这三种成分之间的多重相互作用和反应,无论是直接的还是间接的,都使新电池的发明变得极其困难。必须在这三个组成部分之间进行彻底的平衡,通过仔细设计、选择和集成,同时优化几个关键性能指标(能量和功率密度、循环和日历寿命、效率、安全性和成本)。惰性成分(隔膜、电极基板和添加剂)的存在使事情进一步复杂化,因为它们在化学层面并不是真正的惰性。
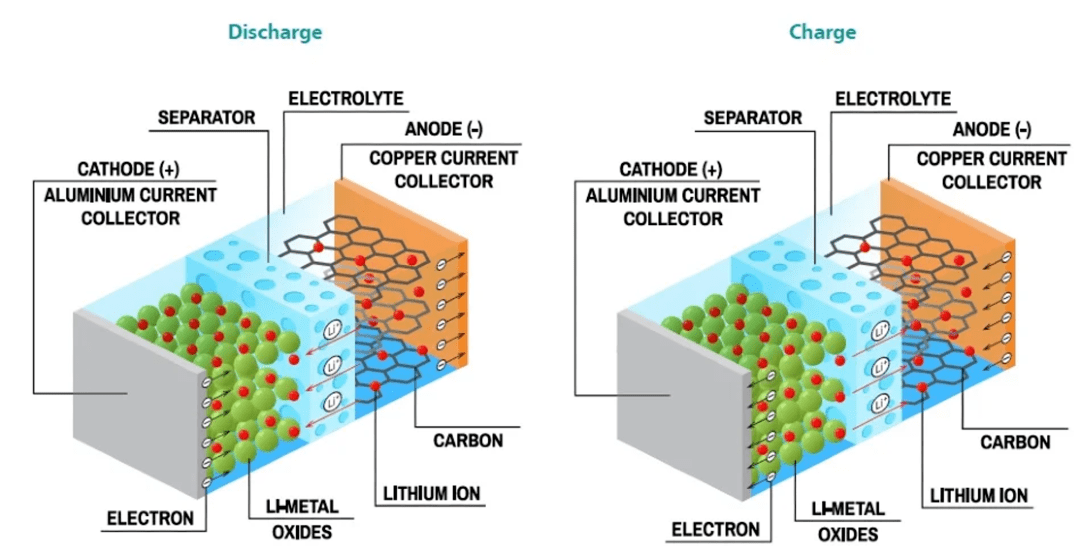
锂离子电池能够在过去三十年里不断进步,很大程度上是得益于消费电子与新能源汽车的巨大需求。然而在没有突破性的技术出现之前,我们很难逾越元素与化学反应本身的限制,电池容量也必将受限于此,成为我们这个时代的阿喀琉斯之踵。